Austrotransplant 2018
32. Tagung der Österreichischen Gesellschaft für Transplantation,Transfusion und Genetik
Die Zukunft der Organtransplantation
Eine Niere aus dem 3D-Drucker, ein Herz, das außerhalb des Körpers künstlich am Leben gehalten wird, und eine Insulinpumpe statt einer Bauchspeicheldrüse. Was im ersten Moment wie eine Utopie klingt, wird von 17. – 19. Oktober in Linz von den führenden österreichischen Transplantationsexperten diskutiert.
Beim Versagen von Organen ist die Transplantation mittlerweile ein fixer Bestandteil der Behandlung, der zu sehr guten und dauerhaften Ergebnissen führt. Das Beispiel der Nierentransplantation zeigt, dass die Funktionsrate mit einem neuen Organ mittlerweile sehr hoch ist. Sie liegt bei Lebendspenden bei 80%, bei postmortalen Spenden bei 70% bei einer 5jährigen Nachsorgezeit.
Erfolgsmodell Nierentransplantation
Menschen, die an Nierenversagen leiden, müssen eine sehr belastende und zeitaufwendige Dialysebehandlung über sich ergehen lassen, und das oft jahrelang. Die einzige Hoffnung auf ein relativ beschwerdefreies Leben ist für sie die Aussicht auf die Transplantation einer gesunden Niere.
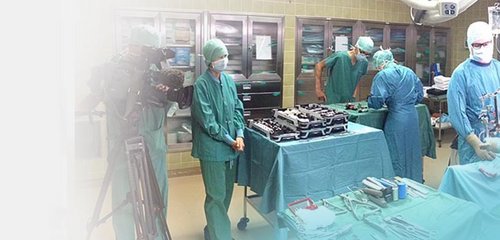
Die Transplantation einer Niere ist eine hoch komplexe Behandlung, die in Österreich nur an vier Zentren durchgeführt wird: an den Universitätskliniken Wien, Graz und Innsbruck sowie im Ordensklinikum Linz Elisabethinen. Für eine erfolgreiche Transplantation ist höchstes chirurgisches Können gefordert, sowohl während der Entnahme der Niere beim Spender, als auch im Zuge des Implantierens des Organs beim Empfänger.
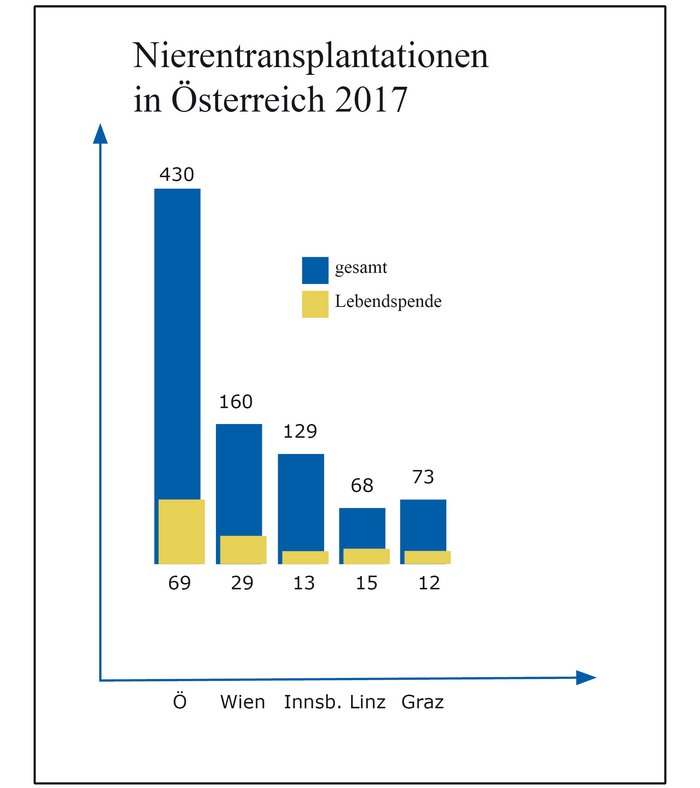
Wartezeit und Nierenspende
Patienten, die eine Nierenspende benötigen, werden im Transplantationsregister von Eurotransplant registriert und erhalten eine passende Niere eines verstorbenen Spenders, sobald ein passendes Organ verfügbar ist. Die Wartezeit auf eine Niere beträgt in Österreich rund drei Jahre. Wesentlich verkürzt kann diese Wartezeit durch eine Lebendspende werden. Dabei stellt ein lebender Spender eine seiner beiden gesunden Nieren zur Verfügung.
In Österreich warten derzeit zirka 1000 Menschen auf ein Organ..
Die Verfügbarkeit von Spender-Organen ist in Österreich im internationalen Vergleich auf einem sehr guten Niveau. Dennoch versterben nach wie vor Menschen, die auf einer Warteliste für ein Spender-Organ stehen und nicht rechtzeitig transplantiert werden können.
Das Ziel der Transplantationsmedizin ist es daher, die Verfügbarkeit von Organen weiter zu verbessern. In Österreich wurden im Jahr 2017, 373 mögliche Organspender gemeldet und davon 206 Fälle realisiert.
Neben der Organ-Spende Verstorbener ist vor allem die Lebendspende eine realistische Strategie, um mehr Organe transplantieren zu können.
„Bei der Jahrestagung diskutieren wir vor allem auch Alternativen, mit dem Ziel, mehr Organe mit guter Qualität zur Verfügung zu haben“ ,erörtert Prim. Dr. Daniel Cejka die Strategie der Transplantationsmediziner.
Alternativen für die Zukunft
Tissue Engineering
Organe aus dem Labor – mit dem 3D-Drucker produziert
Zu den Hauptproblemen der Transplantationsmedizin gehören die Abstoßungsreaktionen, mit denen das Empfängerimmunsystem auf das neue Organ reagiert. Es analysiert das neue Organ als fremd und attackiert es. Die Suche nach einem passenden Spender, dessen Immunsystem zu dem des Empfängers passt, dauert oft sehr lange. Aber auch dann muss der Patient lebenslang immunhemmende Medikamente nehmen.
Könnte ein neues Organ aus den eigenen Zellen gezüchtet werden, würde das Problem nicht auftreten, und auch auf die immunhemmenden Medikamente könnte verzichtet werden.
Ein komplettes Organ im Labor zu züchten ist bisher aber noch nicht möglich. Es gibt aber eine Alternative. Organe wie die Niere bestehen nämlich aus lebenden Zellen, die auf einem Gerüst sitzen. Wenn man nur das Gerüst vom Spender nimmt und es mit den körpereigenen Zellen des Patienten besiedelt, würde ein neues Organ entstehen, das vom eigenen Immunsystem als nicht fremd wahrgenommen und daher nicht bekämpft wird.
Erste Erfolge mit vielversprechenden Ergebnissen verzeichnet diese Technologie bei der Reproduktion von Herzklappen, ein Vorteil, der vor allem beim Einsatz in Kinderherzen relevant ist, weil das künstlich erzeugte Gewebe mit dem natürlichen Gewebe mitwächst.
Maschinenperfusion
Das Herz, das ohne Körper schlägt
Der Erfolg einer Transplantation hängt neben der Verfügbarkeit vor allem von der Qualität des Organs ab. Im Normalfall werden bei einer Herztransplantation der Spender und der Empfänger gleichzeitig auf den Eingriff vorbereitet, sodass es zu keinen Verzögerungen kommt, die das Herz schädigen könnten. Mitunter dauert diese Vorbereitung beim Empfänger aber wesentlich länger als geplant, weil das Öffnen des Brustkorbes wegen Vorerkrankungen unverhältnismäßig lange dauert und das Organ nicht planmäßig eingebaut werden kann.
Bei derartigen Verzögerungen, und auch wenn die Entnahme des Herzens geografisch weit von der Klinik, in der implantiert werden soll, entfernt ist, beginnt ein Wettlauf gegen die Uhr. In der Regel wird ein explantiertes Herz bis zur Öffnung der Hauptschlagader im Empfänger nicht durchblutet. Nachdem die Vene und die Aorta durchtrennt wurden, wird das Organ in eine spezielle Flüssigkeit gelegt und dann auf 4 Grad heruntergekühlt. Dadurch wird der Zellstoffwechsel gebremst und der Muskelkonserviert, damit er nicht gleich abstirbt. In diesem Zustand kann ein Organ zirka 3 Stunden verbleiben, ohne Schaden zu nehmen.
Bei der Maschinenperfusion kann die Zeit bis zur Einpflanzung wesentlich verlängert werden. Dabei wird das entnommene Herz mittels Schläuchen an einen künstlichen Blutkreislauf angeschlossen. Das Gerät, das das Organ mit warmem, sauerstoffreichem Blut des Spenders versorgt, verlängert aber nicht nur die Transportzeit, sondern ermöglicht dem Arzt sogar die Untersuchung mittels Echokardiografie. Die Funktionsweise der Herzklappen kann beispielsweise mit Ultraschallbildern direkt überprüft werden. Für den Chirurgen sind diese Informationen von großer Wichtigkeit bei der Beurteilung der Qualität des Organs.
Die Maschinenperfusion kommt nicht nur bei transplantierten Herzen zum Einsatz, sondern auch bei Leber, Niere und Lunge.
Künstliches Organ
Insulinpumpe statt Bauchspeicheldrüse
Austauschen was nicht mehr funktioniert, ist die Grundidee bei der Transplantation. Allerdings nur, wenn es keine Alternative gibt und sich der Defekt nicht anders beheben lässt. Bei der Bauchspeicheldrüse wird eine andere Strategie verfolgt. Statt das Organ zu ersetzen, wird ihre Funktion, das Gewebe mit Insulin zu versorgen, von einem medizintechnischen Gerät übernommen.
Derartige Geräte überprüfen selbstständig und regelmäßig den Zucker und geben über eine Pumpe das Insulin an den Körper ab. Ein Minicomputer, der an einen Sensor angeschlossen ist, errechnet die richtige Dosis.
Der Vorteil der künstlichen Bauchspeicheldrüse besteht in der Präzision, mit der der Computer arbeitet. Seine Ergebnisse können manuell nicht annähernd erreicht werden. Damit kann der Blutzucker wesentlich stabiler gehalten werden. Besonders in der Nacht, kann diese Technik der gefährlichen Unterzuckerung, die bei Typ-1-Diabetes auftritt, vorbeugen.
Ihre Ansprechspartner sind:
Prim. Doz. Dr. Daniel Cejka, Ordensklinikum Linz – Elisabethinen, Leiter der Abteilung für Nephrologie und Transplantationsmedizin am Ordensklinikum Linz Elisabethinen, Kongresspräsident
Prof. Dr. Robert Langer, Leiter der Transplantationsgruppe im Ordensklinikum Linz Elisabethinen, Kongresspräsident
Prim. Prof. Dr. Marcus Säemann, Facharzt für Nieren & Diabetes, Wien
Kontakt und Information:
Ordensklinikum Linz Elisabethinen
Ing. Mag. Günther Kolb
+43-(0)732-7676-2235
guenther.kolb@ordensklinikum.at